Novembre 2024
Cibler certains peptides intestinaux impliqués dans la régulation de l’appétit et le contrôle de la prise alimentaire : tel est le principe des derniers traitements de l’obésité largement médiatisés ces dernières années pour leurs effets significatifs obtenus. Si ces molécules ciblent essentiellement le métabolisme du GLP-1, d’autres peptides intestinaux font l’objet de recherches prometteuses.
Le Glucagon Like Peptide 1 (GLP-1), sécrété lors de l’arrivée de nutriments dans le tube digestif, est un inhibiteur de la prise alimentaire. Cet effet résulte d’une action anorexigène provoquée lors de la liaison du GLP-1 sur son récepteur au niveau du système nerveux central. Le GLP-1 agit également au niveau du système digestif où il entraîne le ralentissement de la vidange gastrique. Il intervient également dans le contrôle glycémique en stimulant la sécrétion d’insuline et en inhibant celle de glucagon. Les recherches pour mettre au point des traitements contre l’obésité – et le diabète de type 2 – ont eu pour objectif de développer des molécules mimant les effets du GLP-1 (ou agonistes) mais présentant une demi-vie [1] plus importante. C’est le cas du liraglutide et du sémaglutide, commercialisés depuis 2014 aux Etats-Unis et 2015 en Europe.
Neutraliser la ghréline, l’hormone de la faim
Les recherches dans les laboratoires pharmaceutiques se poursuivent désormais pour mettre au point des molécules ciblant d’autres peptides intestinaux impliqués dans la régulation de la prise alimentaire. A commencer par la ghréline. Surnommé hormone de la faim, ce peptide de 28 acides aminés stimule l’appétit. Produit au niveau de l’estomac (fundus gastrique), il rejoint la circulation sanguine et atteint l’hypothalamus. Son action conduit à l’inhibition d’une population de neurones anorexigènes, les neurones POMC (voir Figure)… d’où une sensation de faim.
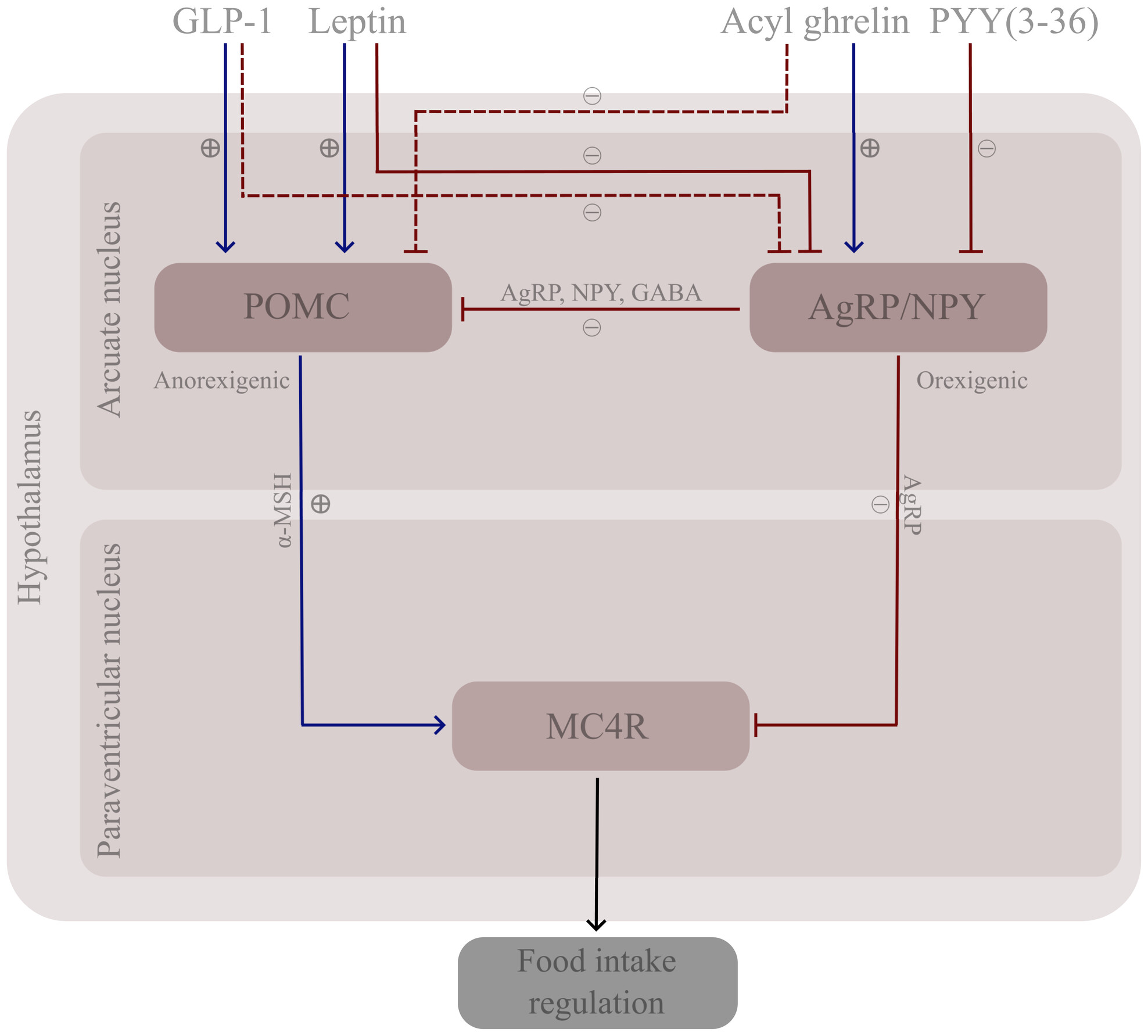 Régulation hypothalamique de la prise alimentaire
Régulation hypothalamique de la prise alimentaire
La ghréline agit aussi sur les circuits cérébraux de la récompense, intensifiant le désir pour des aliments de haute densité énergétique. Cette double action fait de la ghréline un puissant driver de la prise alimentaire. Le développement de molécules ciblant le métabolisme de la ghréline va bien au-delà de la seule prise en charge clinique de l’obésité : de telles molécules pourraient présenter un intérêt pour le traitement d’autres maladies incluant l’anorexie, les troubles de l’addiction, les maladies cardiovasculaires et certaines maladies neurologiques (épilepsie) ou neurodégénératives (Alzheimer, Parkinson) etc. Plusieurs pistes de recherche sont l’objet de travaux, en particulier :
- la neutralisation de la ghréline circulante (grâce à des anticorps ou des séquestrants),
- le développement d’antagonistes du récepteur de la ghréline (ce qui bloque l’action de la ghréline en l’empêchant de se lier à son récepteur)
-
et le développement d’inhibiteurs de l’enzyme GOAT (pour Ghrelin O-acyltransferase), qui transforme la ghréline en sa forme active.
Toutefois, les défis qui restent à relever pour contrer cette hormone à la régulation complexe et aux fonctions contrastées dans l’organisme restent nombreux.
S’inspirer des inhibiteurs naturels de la prise alimentaire, et les optimiser
Contrairement à la ghréline, orexigène, les trois autres peptides intestinaux ciblés par les molécules pharmacologiques en cours de développement sont des inhibiteurs de la prise alimentaire.
- Le peptide YY (PYY) est sécrété par les cellules intestinales lors de l’arrivée des nutriments dans la lumière intestinale. Les individus obèses affichent des taux réduits de PYY (on estime que l’apport calorique requis pour atteindre des taux de PYY semblables à ceux d’individus d’IMC normal est deux fois plus important !). Quand il arrive au cerveau, PYY agit en levant l’inhibition des neurones POMC, libérant ainsi leur action anorexigène. Les stratégies pharmaceutiques visent essentiellement ici à développer des analogues de PYY, mimant ses effets mais plus stables dans le temps et présentant moins d’effets secondaires (ex. nausées) que la forme naturelle quand elle est administrée. En outre, si les essais menés sur modèles animaux avec des analogues de PYY sont encourageants, les essais cliniques peinent à reproduire ces effets chez l’Humain.
- La cholécystokinine (CCK), largement impliquée dans l’absorption intestinale des lipides, est un autre peptide crucial pour l’inhibition de l’appétit. Toutefois, ses rôles physiologiques très diversifiés dans l’organisme, son existence sous différentes formes (environ 80 formes différant par le nombre d’acides aminés du segment terminal de la molécule) ainsi que des effets indésirables observés lors d’essais cliniques menés avec des agonistes des récepteurs CKK sont autant de verrous qui restent à lever dans le développement de molécules pharmaceutiques ciblant le métabolisme de la CKK.
- Enfin, le développement de molécules s’inspirant de l'amyline, très impliquée à la fois dans la régulation glycémique et dans l’inhibition de la prise alimentaire, souffre des mêmes freins ; toutefois, des agonistes d’un double récepteur de l'amyline et de la calcitonine (DACRAs), ainsi que les combinaisons DACRAs/semaglutide (un analogue du récepteur de l’amyline couplée à un analogue du GLP-1) semblent prometteurs, avec des essais cliniques en cours chez l’Humain.
[1] Après l’administration d’un médicament, la demi-vie correspond au temps nécessaire pour que sa concentration plasmatique diminue de moitié