Juillet 2025La perception gustative des composés à saveur sucrée repose sur un récepteur présent dans les bourgeons gustatifs de la langue, composé de deux sous-unités : TAS1R2 et TAS1R3 (Figure). Des variations de séquence d’ADN au niveau des gènes codant pour ces sous-unités – qui modifient la séquence protéique et donc la conformation spatiale du récepteur – sont suspectées d’être impliquées dans l’altération de la perception sucrée, voire dans certains comportements alimentaires et phénotypes tels que l’obésité. Dans le cadre d’un projet européen plus vaste (SWEET), une équipe du Centre des Sciences du Goût et de l’Alimentation (CSGA) à Dijon a imaginé un dispositif in vitro permettant de tester l’effet réel de telles variations génétiques sur la fonctionnalité du récepteur.
Une trentaine de variants génétiques testés
Pour cela, ils ont fait exprimer à des cellules humaines des récepteurs gustatifs codés par différents variants génétiques (dits SNP pour single-nucleotide polymorphism, c’est-à-dire des variants ne se différant que par un seul nucléotide dans la séquence d’ADN) : 12 variants génétiques de la sous-unité TAS1R2 et 16 variants génétiques de la sous-unité TAS1R3. L’activité fonctionnelle de ces récepteurs en réponse à 12 édulcorants était ensuite testée en mesurant les variations du calcium intra-cellulaire (l’activation du récepteur TAS1R2/TAS1R3 déclenche une cascade de réactions intra-cellulaires qui aboutit à une augmentation du calcium dans le cytoplasme).
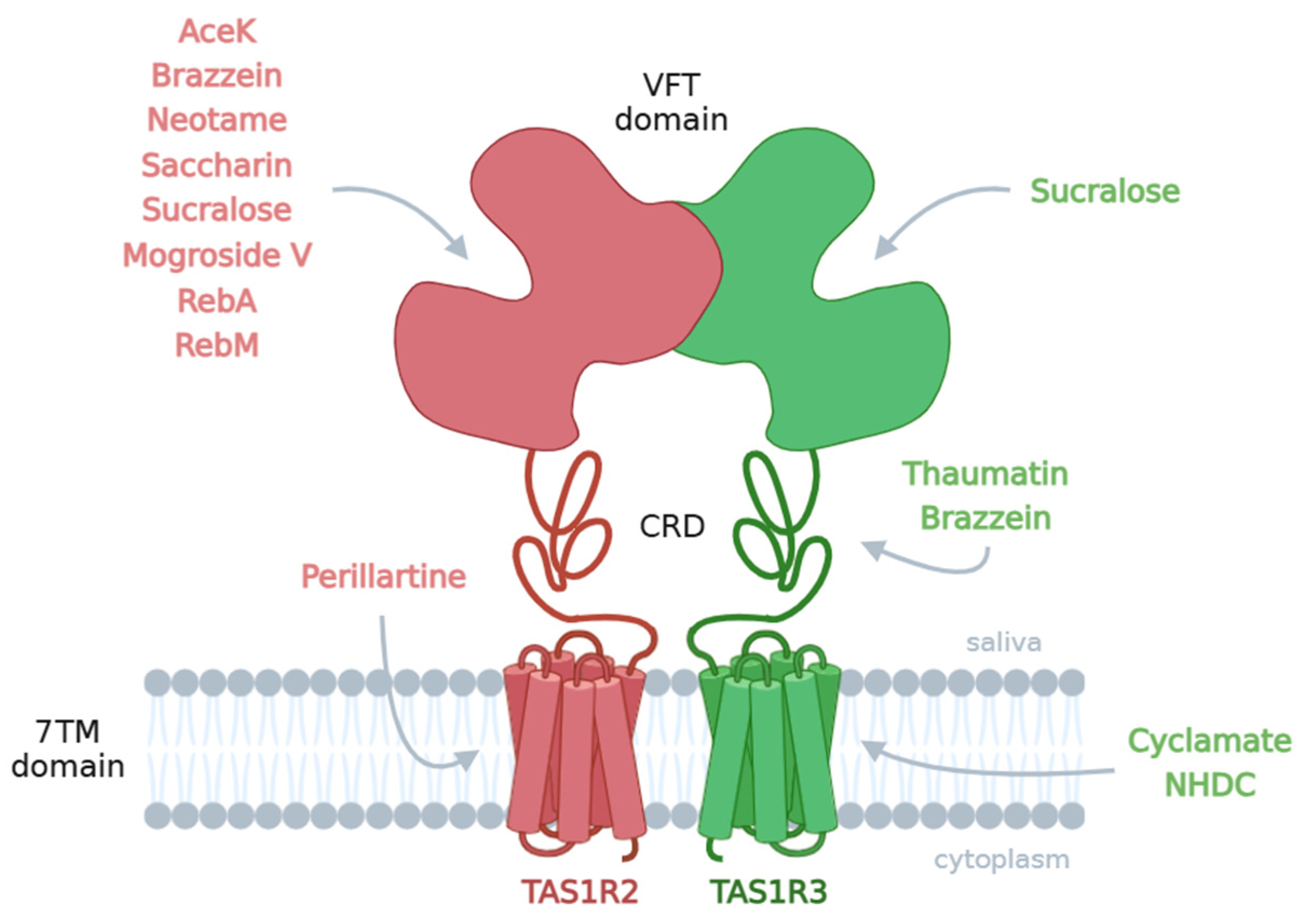
Le récepteur de la saveur sucrée exprimé par les cellules gustatives est composé de deux sous-unités (TAS1R2/TAS1R3) présentant des sites de liaisons pour de nombreux composés.
Des récepteurs plus ou moins fonctionnels
Ce dispositif a permis aux chercheurs d’identifier 2 variants génétiques du TAS1R2 et 5 variants du TAS1R3 conduisant à une altération de l’activité fonctionnelle du récepteur en réponse à la plupart des édulcorants, par rapport au variant de référence (i.e. allèle le plus fréquent dans la population). À l’inverse, certains variants de TAS1R3 conduisaient à une amélioration de l’activité fonctionnelle. Cela suggère que ces variants SNP entraînent une modification de la structure du récepteur à même d’impacter sa fonctionnalité. Pour autant, les variants génétiques connus pour être associés à certains comportements/phénotypes (ex. apports en sucres) ne modifiaient pas la fonctionnalité du récepteur. Pour les chercheurs, aucun lien clair ne ressort ainsi entre des phénotypes humains et la réponse cellulaire à des SNP spécifiques, suggérant l’implication d’autres facteurs (environnementaux, comportementaux ou génétiques autres que TAS1R2/TAS1R3) dans la formation des préférences et consommations sucrées.
Des variants spécifiques en cas de surpoids/d’obésité ?
En parallèle de ces travaux in vitro, les chercheurs ont utilisé des échantillons d’ADN sanguin obtenus auprès de 162 personnes en situation de surpoids/obésité (IMC entre 25 et 35 kg/m²) pour identifier des variants présents/surreprésentés dans cette population et susceptibles d’impacter la fonctionnalité du récepteur. Sept nouveaux variants engendrant une perte de fonction probable [1] du récepteur de la saveur sucrée ont été identifiés dans cette population, à une fréquence plus élevée que dans la population générale. Ces variants n’avaient pas encore été identifiés dans la littérature comme associés à la fonctionnalité du récepteur ou certains phénotypes comme l’obésité. Toutefois, la faible taille de l’échantillon, jugé non représentatif, limite la généralisation de la portée de ces résultats à l’ensemble des patients en surpoids/obèses. Les chercheurs soulignent la nécessité d’études à plus grande échelle, mettant en relation des données génétiques, la fonctionnalité biologique du récepteur et des données comportementales (sensibilité gustative, appétence et consommations sucrées).
[1] impact prédit grâce à des outils bio-informatiques au vu du type de SNP