Mai 2026Longtemps cantonné à un simple rôle de réservoir énergétique, le tissu adipeux blanc [1] est aujourd’hui considéré comme un véritable organe immuno-métabolique. Une revue de littérature menée par des équipes de recherche françaises examine les mécanismes à travers lesquels les adipocytes participent activement à la régulation de l’inflammation, du métabolisme et de l’homéostasie tissulaire.
En effet, les adipocytes ne se contentent pas de stocker des lipides ; ils sécrètent de nombreux médiateurs (adipokines, vésicules extra-cellulaires) capables d’interagir avec le système immunitaire. En situation d’obésité, cette propriété des adipocytes contribue au développement d’une inflammation de bas grade, désormais reconnue comme un déterminant majeur de l’insulino-résistance et des maladies métaboliques. La figure 1 met par exemple en lumière le rôle joué par l’augmentation de la sécrétion de leptine par le tissu adipeux et la diminution de celle d’adiponectine [2] dans le développement d’un état inflammatoire, lors de l’expansion du tissu adipeux.
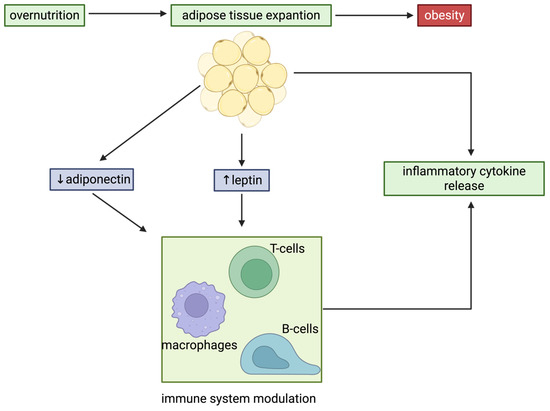 Figure 1 : Inflammation induite par la leptine lors de l’expansion du tissu adipeux
La surcharge énergétique chronique favorise l’expansion du tissu adipeux, entraînant une augmentation de l’expression et de la sécrétion de leptine par les adipocytes. La leptine d’origine adipocytaire stimule la production de cytokines pro-inflammatoires par les cellules immunitaires, créant ainsi un environnement inflammatoire qui contribue à la dérégulation métabolique systémique. Parallèlement, la sécrétion d’adiponectine par les adipocytes, une adipokine aux propriétés anti-inflammatoires, diminue.
Figure 1 : Inflammation induite par la leptine lors de l’expansion du tissu adipeux
La surcharge énergétique chronique favorise l’expansion du tissu adipeux, entraînant une augmentation de l’expression et de la sécrétion de leptine par les adipocytes. La leptine d’origine adipocytaire stimule la production de cytokines pro-inflammatoires par les cellules immunitaires, créant ainsi un environnement inflammatoire qui contribue à la dérégulation métabolique systémique. Parallèlement, la sécrétion d’adiponectine par les adipocytes, une adipokine aux propriétés anti-inflammatoires, diminue.
Une inflammation à double visage
L’inflammation du tissu adipeux ne doit cependant pas être perçue uniquement comme délétère. À court terme, une réponse inflammatoire contrôlée participe au remodelage du tissu, notamment lors de variations de poids. Elle permet l’adaptation du tissu adipeux en facilitant le renouvellement des adipocytes.
En revanche, dans un contexte de surcharge énergétique chronique (cf. figure 2), les adipocytes hypertrophiés, soumis à un stress métabolique et à une hypoxie locale, adoptent un profil pro-inflammatoire. Ils recrutent alors des cellules immunitaires et entretiennent un état inflammatoire chronique, délétère pour la fonction métabolique.
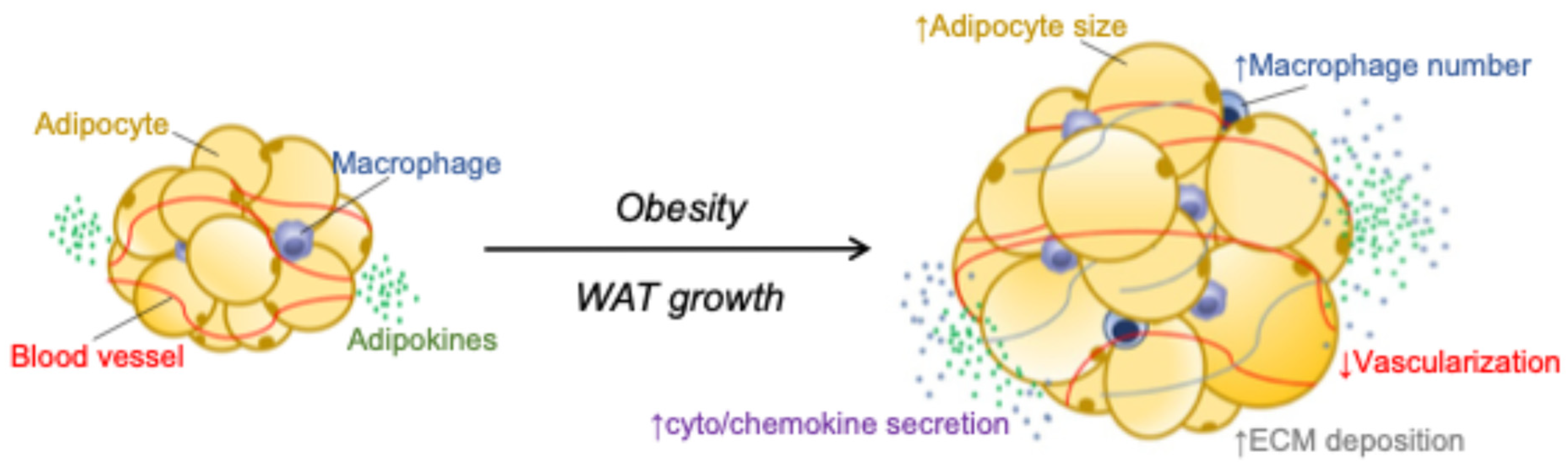 Figure 2 : Remodelage du tissu adipeux en situation d’obésité
La figure met en évidence le basculement d’un tissu adipeux « sain », caractérisé par un équilibre immunitaire et une bonne fonctionnalité des adipocytes vers un tissu désorganisé en situation d’excès énergétique chronique. Les adipocytes augmentent de taille, la sécrétion de médiateurs devient anormale et l’environnement cellulaire se transforme. Tout particulièrement, les cellules immunitaires pro-inflammatoires deviennent majoritaires. Parallèlement, le tissu se rigidifie sous l’effet de la fibrose, limitant ainsi sa capacité d’expansion et entretenant l’inflammation.
Figure 2 : Remodelage du tissu adipeux en situation d’obésité
La figure met en évidence le basculement d’un tissu adipeux « sain », caractérisé par un équilibre immunitaire et une bonne fonctionnalité des adipocytes vers un tissu désorganisé en situation d’excès énergétique chronique. Les adipocytes augmentent de taille, la sécrétion de médiateurs devient anormale et l’environnement cellulaire se transforme. Tout particulièrement, les cellules immunitaires pro-inflammatoires deviennent majoritaires. Parallèlement, le tissu se rigidifie sous l’effet de la fibrose, limitant ainsi sa capacité d’expansion et entretenant l’inflammation.
Un tissu adipeux hétérogène
Un élément clé pour la pratique clinique est l’hétérogénéité du tissu adipeux. Pour un même poids, certaines sous-populations d’adipocytes conservent une bonne sensibilité à l’insuline, tandis que d’autres contribuent davantage à l’inflammation. La localisation des dépôts adipeux est également déterminante. La graisse viscérale apparaît plus active sur le plan inflammatoire, notamment via la libération de vésicules extra-cellulaires, susceptibles d’influencer à distance d’autres tissus.
Hypoxie, rigidité et inflammation : un cercle vicieux
L’expansion du tissu adipeux entraîne une diminution de l’oxygénation locale. Cette hypoxie favorise un remodelage fibro-inflammatoire du tissu, avec une tendance à la fibrose [3] et à la rigidification. Cette perte de plasticité limite la capacité du tissu à s’adapter et entretient l’inflammation.
Par ailleurs, certaines boucles métaboliques auxquelles participent les adipocytes, impliquant des métabolites tels que la glutamine ou le lactate, peuvent auto-entretenir cet état inflammatoire. En conséquence, cette inflammation peut persister même après une perte de poids, traduisant une mémoire tissulaire défavorable.
Quelles implications pour la prise en charge ?
En pratique, ces données invitent à dépasser une approche centrée uniquement sur le poids et à prioriser une amélioration de la qualité et de la fonctionnalité du tissu adipeux. Plusieurs leviers se dégagent dans l’objectif de maintenir la plasticité du tissu adipeux, permettant d’obtenir une réponse adaptée aux variations des stress nutritionnels auxquels les patients en situation d’obésité sont confrontés :
- cibler prioritairement la graisse viscérale (mesure du tour de taille) qui a un impact inflammatoire plus important que le seul poids corporel ;
- favoriser une meilleure oxygénation du tissu par le mouvement ;
- intégrer le rôle du sommeil et de l’alimentation dans la régulation inflammatoire ;
- maintenir un suivi métabolique prolongé, y compris après amaigrissement.
Il est également essentiel d’expliquer aux patients que l’inflammation n’est pas systématiquement négative : c’est sa chronicité qui devient pathologique.
[1] Le tissu adipeux blanc constitue la grande majorité des masses graisseuses de l’organisme. Il participe à la régulation du métabolisme énergétique en stockant et en libérant l’énergie. Le tissu adipeux brun, quant à lui, dissipe l’énergie sous forme de chaleur via la thermogenèse et contribue ainsi à la régulation de la température corporelle.
[2] L’adiponectine est une adipokine (sécrétée par les adipocytes) ayant des propriétés bénéfiques sur le
métabolisme du glucose, le stress oxydatif, l’athérogenèse et l’inflammation chronique. Sa sécrétion est
diminuée en cas de diabète de type 2, d’obésité, d’hypertension artérielle et de syndrome métabolique.
[3] Fibrose : Processus conduisant au remplacement des tissus sains par des tissus fibreux qui perdent leur fonctionnalité d’origine.