Avril 2024
Alors que l’obésité est reconnue comme une maladie par l’OMS depuis plus de 20 ans, elle n’est pas toujours considérée ni traitée comme telle. Comprendre en quoi il s’agit d’une maladie est primordial pour assurer une meilleure prise en charge… et déconstruire certaines idées reçues préjudiciables. C’est dans cet objectif que deux chercheurs ont repris, dans une revue, les bases physiologiques de la régulation de la masse grasse et les dérèglements observés au cours de l’obésité.
Masse grasse : un état d’équilibre défendu par l’organisme…
Dans un état physiologique (non pathologique), notre masse grasse évolue de façon assez prévisible tout au long de la vie, avec la perte progressive de la graisse acquise par les bébés au cours de la petite enfance, les changements de la teneur et de la distribution corporelle en graisse au cours de la puberté et de l’avancée en âge, ou encore au cours de la grossesse et de l’allaitement. A chacune de ces étapes de vie, un point d’équilibre physiologiquement déterminé est atteint en termes de masse grasse. De puissants mécanismes de régulation, modulant à la fois la prise alimentaire et la dépense énergétique, s’opposent à tout éloignement de ce point d’équilibre.
… trop élevé en cas d’obésité
Il en va de même en cas d’obésité. Toutefois, dans ce cas, ce système de régulation s’établit à un point d’équilibre trop élevé, correspondant à un niveau de masse grasse excessif, aux effets délétères pour la santé. L’un des objectifs du traitement de l’obésité consiste à repositionner le point d’équilibre à un niveau de masse grasse plus bas. Or, selon les mécanismes de régulation décrits-ci-dessus, tout écart par rapport au point d’équilibre va générer des réponses métaboliques destinées à y retourner : réduction des sensations de satiété, hyperphagie, etc. En aucun cas, ces symptômes ne peuvent et ne doivent donc être considérés comme un manque de volonté ou de la gloutonnerie de la part des patients, idées reçues qui circulent malheureusement encore couramment.
En réalité, ces comportements alimentaires sont sous le joug de systèmes de régulation pluriels et complexes, orchestrés par différentes zones cérébrales, en communication avec les organes périphériques tels que l’intestin, mais aussi le tissu adipeux.
Deux systèmes hormonaux complémentaires
Lorsque nous mangeons, les aliments libèrent des nutriments qui rejoignent la circulation sanguine et peuvent directement stimuler les circuits neuronaux cérébraux modulant le comportement alimentaire. Ils sont également détectés par des capteurs intestinaux, ce qui déclenche la sécrétion d’une myriade d’hormones elles-mêmes capables de d’influer sur l’activité des zones cérébrales impliquées dans la satiété. Parmi ces hormones, on peut citer l’insuline, ou encore le peptide YY. A l’opposé, la ghréline qui stimule l’appétit, est inhibée.
En parallèle de ces régulations liées à l’arrivée de nutriments dans l’organisme, un second système opère. Son rôle ? Rendre compte de l’état des réserves de graisses de l’organisme. Son existence, pressentie dès les années 1950, n’a été réellement établie que dans les années 90 avec la découverte de son principal effecteur : la leptine. Cette hormone dite "anorexigène", sécrétée par les cellules adipeuses, est capable de traverser la barrière hémato-encéphalique et de de se lier aux récepteurs de l’hypothalamus, modulant ainsi à la fois la prise alimentaire, la dépense énergétique et la masse grasse.
Un système homéostatique sophistiqué
Les différents signaux provenant de l'intestin et du tissu adipeux convergent vers différents centres cérébraux qui intègrent en permanence des informations sur l’état de jeûne, les calories consommés et la masse grasse, et génèrent une réponse orientant la prise alimentaire et la dépense énergétique. Trois zones cérébrales sont impliquées : le tronc cérébral, les circuits de la récompense, et l’hypothalamus.
Au sein de ce dernier, les rôles antagonistes de deux populations de neurones ont été particulièrement bien décrits : les neurones POMC[1] d’une part, les neurones NPY/AgRP[2] d’autre part. Les premiers, qui s’activent sous l’effet de l’insuline et de la leptine, inhibent la prise alimentaire et augmentent la dépense énergétique ; les seconds, stimulés par la perte de poids, la ghréline ou le jeûne, agissent à l’opposé.
Ainsi, à l’instar d’autres systèmes homéostatiques qui régissent les processus vitaux comme le contrôle de la pression artérielle, de la glycémie ou de l’équilibre électrolytiques, ce système sophistiqué régule la masse grasse sans intervention consciente, en générant des sensations de faim ou de satiété, et probablement même en influençant la motivation à être actif. C’est d’ailleurs ce réseau cérébral qui constitue la cible des médicaments développés pour traiter l’obésité.
L’obésité comme conséquence d’une résistance à la leptine
Ce système bien « huilé » connaît pourtant parfois des dérégulations. La prise de poids est suspectée d’être liée à des dérégulations de la signalisation de la leptine et/ou des hormones intestinales, conduisant à l’établissement d’un nouveau point d’équilibre de la masse grasse, plus élevé. Une dégradation de l’activation des récepteurs neuronaux par ces hormones ou de la transduction serait en cause. A l’instar de l’insulinorésistance qui signe les phases précoces du diabète de type 2, les chercheurs estiment qu’une résistance à la leptine se mettrait en place au cours du développement de l’obésité
(Figure) : la moindre capacité de la leptine à activer les circuits cérébraux conduirait à une augmentation de sa production par le tissu adipeux via l’expansion de celui-ci. L’élévation des taux de leptine observée en cas de l’obésité serait ainsi secondaire à la résistance qui se met en place.
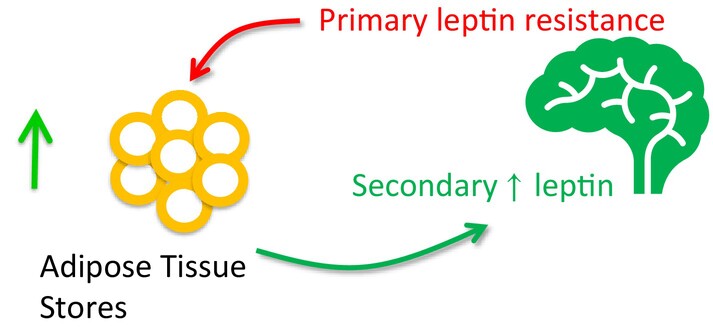 L'apparition d'une résistance à la leptine entraînerait une expansion des réserves adipeuses, augmentant ainsi les niveaux de leptine jusqu’à contrecarrer la résistance des tissus.
L'apparition d'une résistance à la leptine entraînerait une expansion des réserves adipeuses, augmentant ainsi les niveaux de leptine jusqu’à contrecarrer la résistance des tissus.
La surconsommation alimentaire qui se produit au cours de ce processus est considérée à la fois comme une conséquence et un médiateur de la maladie. Lorsque un taux de leptine permettant de restaurer la signalisation neuronale est atteint (via l’extension du tissu adipeux), le poids se stabilise, avec une balance énergétique et une masse grasse qui s’établissent à un nouveau point d’équilibre… férocement défendu par l’organisme contre toute tentative de retour à l’état précédent.
Mais comment expliquer l’origine des dérégulations observées en cas d’obésité ? Comme la plupart des maladies chroniques, l’obésité résulte d’une interaction entre facteurs génétiques et environnementaux. Plus la maladie prend une forme précoce et sévère, plus le poids des facteurs génétiques est important. Et plus la génétique pèse, plus l’appétit est dérégulé. Quant aux facteurs environnementaux, les modes de vie sédentaires et certains composants du régime occidental (riche en graisses, fructose, et aliments ultra-transformés) sont pointés ; leurs effets sur le contrôle central de l’appétit restent à élucider.
Des mécanismes clés pour la compréhension et la prise en charge de l’obésité
Quoi qu’il en soit, la mise en évidence des mécanismes de contrôle de la prise alimentaire et de régulation de la masse grasse étaye la base biologique des comportements alimentaires observés en cas d’obésité (par opposition aux théories mettant en avant des conditions psychologiques comme le binge eating ou le syndrome de l’alimentation nocturne). Ce cadre théorique permet également de comprendre les mécanismes d’action des traitements actuels (médicaments, chirurgie bariatrique) proposés aux patients obèses, et, les auteurs en sont certains, servira de socle au développement des nouvelles stratégies de prévention et de traitement de l’obésité.
[1] Neurones à pro-opiomélanocortine
[2] neuropeptide Y (NPY) et peptide apparenté à l'agouti (AgRP)