Avril 2024
Le diabète de type 2 (DT2) est une maladie hétérogène, à la fois dans sa présentation clinique (âge d’apparition, complications, efficacité des traitements…) et dans les mécanismes à l’œuvre. Or, la part d’héritabilité du DT2 peut atteindre 70 % dans certaines populations, pointant le rôle de prédisposition génétique en sus des facteurs environnementaux et du mode de vie. D’où la nécessité d’identifier les gènes impliqués dans la survenue et à la présentation de la maladie. Des chercheurs publient dans Nature la plus grande étude d'associations pangénomiques[1] à date sur le sujet. Objectif : identifier les variations génétiques associées aux différents phénotypes du DT2.
Plus d’un millier de gènes associés au diabète de type 2
Dans le cadre d’une collaboration internationale, ils ont compilé les données ADN de plus de 2,5 millions de sujets – dont plus de 400 000 sujets atteints de diabète de type 2 –, constituant ainsi un échantillon au moins 3 fois plus grand que ceux des précédentes études. Six origines ethniques étaient représentées : ascendance européenne, d’Asie de l’Est, africo-américaine, hispanique, d’Asie du Sud ou sud-africaine.
Près de 1 300 variations génétiques (allèles), localisées dans plus de 600 régions de l’ADN, sont ressorties comme associées au diabète de type 2 ; 150 de ces régions n’avaient encore jamais été identifiées.
Des groupes de gènes associés au profil métabolique
Les chercheurs ont ensuite exploré les associations entre les allèles identifiés et une série de traits métaboliques : mesures anthropométriques, composition corporelle, réponse glycémique, lipides plasmatiques, etc. Grâce à des techniques de regroupements statistiques, 8 grands clusters d’allèles sont ressortis, chacun s’exprimant dans certaines cellules types (ex : pancréatiques, adipocytes…) et correspondant à un profil cardio-métabolique particulier (Figure).
- Deux clusters, caractérisés par un dysfonctionnement des cellules β-pancréatiques (et donc une capacité altérée à sécréter de l’insuline) étaient associés à une glycémie à jeun plus élevée, un taux d’hémoglobine glyquée plus élevé et une insulinémie à jeun plus faible ;
- Trois clusters, caractérisés par une résistance des tissus à l’insuline, étaient associés aux mesures anthropométriques (IMC et tout de taille plus élevés…) et aux taux de lipides sanguins (dyslipidémie…) ;
- et trois nouveaux clusters d’allèles, non identifiés dans les précédentes études, correspondaient à des particularités métaboliques soit évocatrices du syndrome métabolique, soit touchant spécifiquement la masse grasse, soit reflétant un contrôle glycémique résiduel.
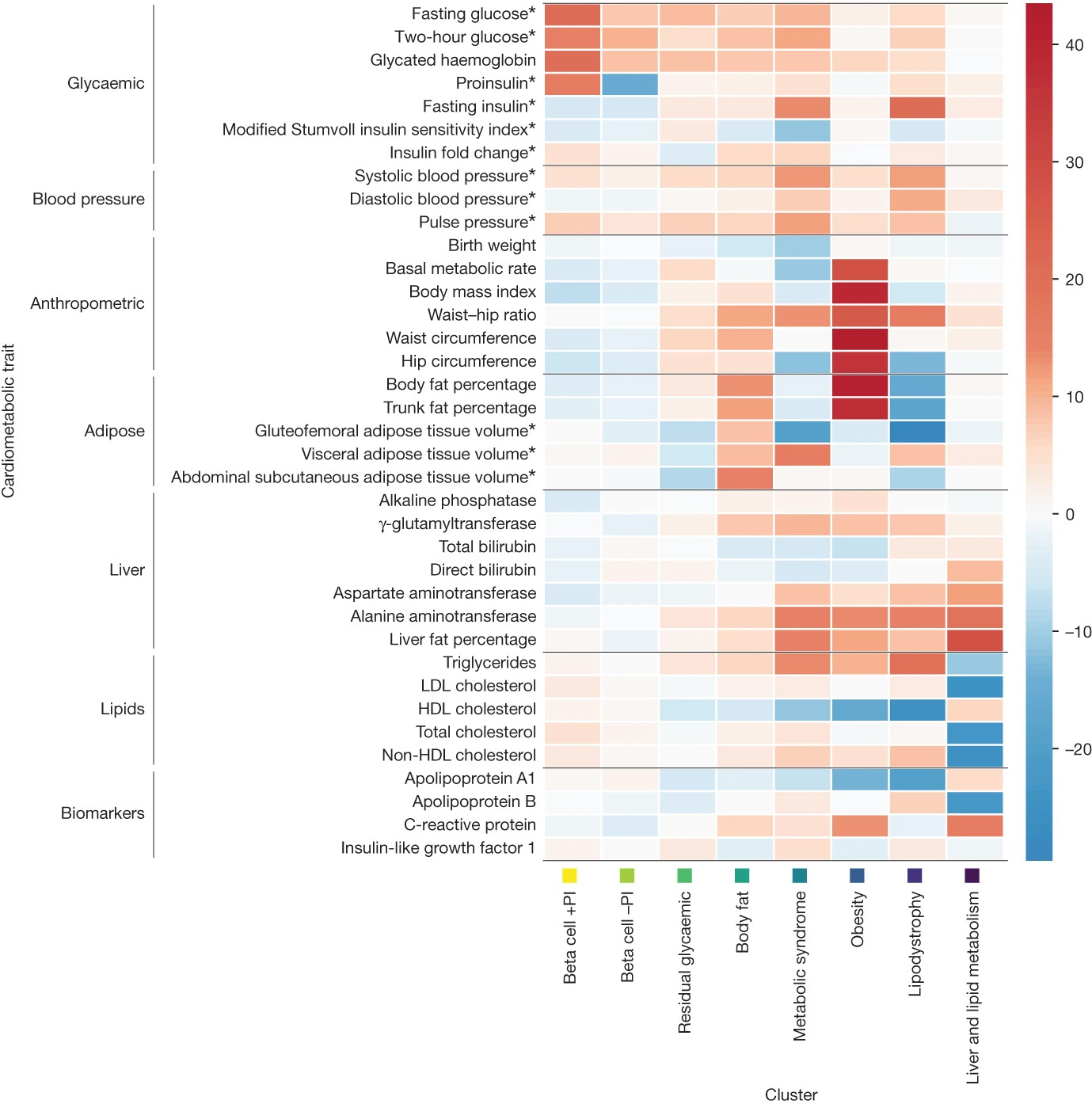 Associations (positives en rouge et négatives en bleu) entre les 8 clusters de gènes associés au diabète de type 2 et les traits cardiométaboliques
Associations (positives en rouge et négatives en bleu) entre les 8 clusters de gènes associés au diabète de type 2 et les traits cardiométaboliques
Vers des prises en charge éclairées par la génétique ?
A travers l’utilisation de scores polygéniques[2] , des associations entre certains clusters d’allèles et le risque de maladies vasculaires (maladie coronarienne, maladie artérielle périphérique, néphropathie diabétique) étaient mises en évidence. Interprétation des chercheurs ? L’existence de mécanismes biologiques communs à certaines formes de DT2 et ces maladies. En perspective de ces travaux, les chercheurs entrevoient la possibilité de développer dans le futur des prises en charge spécifiques du DT2 et de ses complications, tenant compte du profil génétique des patients.
[1] Une étude d'association pangénomique (GWAS pour genome-wide association study en anglais) est une approche utilisée pour identifier les variations génétiques statistiquement associées à un risque de maladie ou à un trait particulier. La méthode consiste à étudier le génome de nombreuses personnes, à la recherche de variantes génétiques qui surviennent plus fréquemment chez les personnes atteintes d'une maladie ou présentant un trait spécifique, par rapport à celles qui n'en souffrent pas.
[2] Mesure d’un risque de maladie lié aux gènes de l’individu